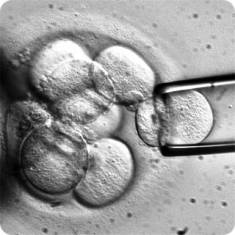
La Agencia Americana del Medicamento (FDA, en sus siglas en inglés) ha aprobado el primer tratamiento oral para las formas recurrentes de la esclerosis múltiple, que será comercializado por Novartis con el nombre de ‘Gilenya’.
La Agencia Americana del Medicamento (FDA, en sus siglas en inglés) ha aprobado el primer tratamiento oral para las formas recurrentes de la esclerosis múltiple, que será comercializado por Novartis con el nombre de ‘Gilenya’.
En Estados Unidos se estima que esta enfermedad neurodegenerativa afecta a más de 400.000 personas y la variante más frecuente es la forma recurrente, que se caracteriza por exacerbaciones o “reactivaciones” intercaladas con periodos de remisión de la enfermedad.
El tratamiento habitual de estos pacientes incluye una dosis frecuente de inyecciones frente a las que esta nueva molécula, cuyo principio activo es fingolimod, supone una “excelente” y “cómoda” alternativa ya que se administra en cápsulas, según ha destacado Nicholas LaRocta, Vicepresidente de Asistencia Sanitaria y Políticas de Investigación de la Sociedad Nacional de Esclerosis Múltiple estadounidense.
Leer más…
 En el cambio más significativo en 25 años a las cajetillas de cigarros en Estados Unidos, las autoridades de salud dieron a conocer el martes nueve etiquetas de nuevas de advertencia que muestran con detalles gráficos los efectos negativos de consumir tabaco.
En el cambio más significativo en 25 años a las cajetillas de cigarros en Estados Unidos, las autoridades de salud dieron a conocer el martes nueve etiquetas de nuevas de advertencia que muestran con detalles gráficos los efectos negativos de consumir tabaco.
 Nuevas investigaciones están indicando una transformación grande en la forma en la que se crean los fármacos para el cáncer y cómo son tratados los pacientes, ofreciendo la promesa de terapias personalizadas que lleguen a los pacientes más rápida y eficazmente que otros medicamentos.
Nuevas investigaciones están indicando una transformación grande en la forma en la que se crean los fármacos para el cáncer y cómo son tratados los pacientes, ofreciendo la promesa de terapias personalizadas que lleguen a los pacientes más rápida y eficazmente que otros medicamentos.
 Del 12 al 13 de junio del 2000 tuvo lugar en Herndon, Virginia, Estados Unidos, un “workshop” titulado “Scientific Evidence on Condom Effectiveness for Sexually Transmitted Disease (STD) Prevention”, para examinar la evidencia científica en lo que respecta al preservativo. En él participaron varias agencias federales de esta nación, que prepararon el resumen que contiene las conclusiones de esas reuniones. Dicho resumen no fue emitido hasta un año después.
Del 12 al 13 de junio del 2000 tuvo lugar en Herndon, Virginia, Estados Unidos, un “workshop” titulado “Scientific Evidence on Condom Effectiveness for Sexually Transmitted Disease (STD) Prevention”, para examinar la evidencia científica en lo que respecta al preservativo. En él participaron varias agencias federales de esta nación, que prepararon el resumen que contiene las conclusiones de esas reuniones. Dicho resumen no fue emitido hasta un año después.